Connaître l'anatomie du porc est le premier point de départ pour mieux appréhender comment Mycoplasma hyopneumoniae exerce son pouvoir pathogène.
Anatomie pulmonaire : les défenses locales en place
Les poumons du porc sont composés de 7 lobes dans lesquels l’air arrive par la trachée qui se ramifie en bronches (une par lobe) puis en bronches secondaires et bronchioles pour aller jusqu’au bout des lobes.
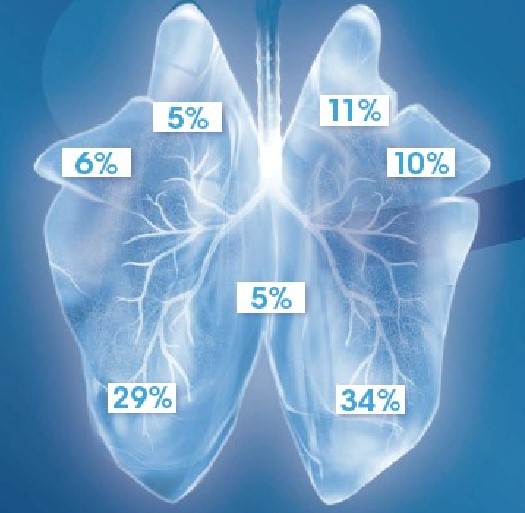
Figure 1 : Représentation schématique d'un poumon de porc avec ses 7 lobes.
Chaque lobe contribue différemment à l’ensemble du volume pulmonaire total.
Ci-dessous leur contribution respective : Apical droit = 11 % / Cardiaque droit = 10 % / Diaphragmatique droit = 34 % / Apical gauche = 5 % / Cardiaque gauche = 6 % / Diaphragmatique gauche = 29 % / Intermédiaire = 5 %.
L’anatomie pulmonaire offre une succession de défenses contre les poussières et pathogènes. Cela commence bien sûr par le groin et les cornets nasaux qui permettent une première filtration et le réchauffement de l‘air. Mais cela continue ensuite. Les surfaces respiratoires sont en effet recouvertes jusqu’aux bronchioles par une couche superficielle de mucus visqueux dont le rôle est de capter les poussières et les pathogènes qui ont réussi à passer les cornets nasaux. Cette couche de mucus n'est pas statique car elle recouvre des cellules ciliées dont les cils sont en perpétuel mouvement pour « remonter » et expulser le mucus. Il a pu être estimé que ces cils permettaient d’évacuer le mucus a une vitesse de quelques millimètres par minute. Le mucus finit alors par rejoindre le larynx et le pharynx puis le cochon le déglutit. C’est ce qu’on appelle l’escalator mucociliaire.
Une première étape : la destruction de l’escalator mucociliaire
La contamination d’un porc par Mycoplasma hyopneumoniae (Mhyo) se fait exclusivement par voie respiratoire. Après avoir passé la cavité nasale, Mhyo se colle sur la couche de mucus qu’il arrive finalement à franchir pour adhérer aux cellules ciliées sous-jacentes. Mhyo est une bactérie extra-cellulaire : c’est donc là, à la surface de la trachée et des bronches, qu’il va se développer.
Son mode d’action d’un point de vue biochimique n’est, à l’heure actuelle, toujours pas complètement élucidé. Comprendre mieux ces mécanismes pourrait pourtant aider à mieux cerner pourquoi certaines souches de Mhyo sont plus pathogènes que d’autres. Néanmoins, plusieurs éléments font consensus.
Une fois accolé aux cils de l’escalator mucociliaire, Mhyo ne produit pas de toxines en tant que tel mais des métabolites qui vont induire un arrêt de l’arbre mucociliaire puis sa destruction. Le peroxyde d’hydrogène (H2O2) fait partie par exemple des métabolites que Mhyo peut produire. On comprend facilement que ce puissant oxydant fasse des dommages à l’escalator mucociliaire ! La toux s’installe alors.
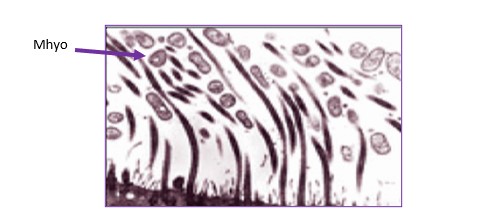
Figure 2 : Action de Mhyo dans l’arbre respiratoire : adhésion de Mhyo aux cils de l’escalator mucociliaire (Bentley 2005).
La destruction de ce système de défense conduit à avoir plus de pathogènes inhalés dans le tissu pulmonaire. Mais cela ne s’arrête pas là car Mhyo finit aussi par moduler à la baisse la réponse immunitaire locale. Moins de défenses physiques, moins de défenses immunitaires locales expliquent alors pourquoi Mhyo favorise les infections secondaires (comme celles à Pasteurelles, un grand classique). Tout cela facilite aussi sa propre persistance dans le poumon. Et ce d’autant plus, qu’il a la capacité à se protéger en se « cachant » dans des biofilms qu’il produit.

Figure 3 : Action de Mhyo sur l'escalator mucociliaire : détail des étapes ( Pr. D. Maes).
La réponse immunitaire de l’hôte composante à part entière de la pathogénicité de Mhyo. La réponse immunitaire et inflammatoire globale induite par Mhyo apparaît désormais comme une composante à part entière de la pathogénicité de Mhyo, si ce n’est la première composante. Elle repose sur une production de cytokines pro-inflammatoires et de cytokines anti-inflammatoires dont le déséquilibre contribue à la pathologie respiratoire. Nous pouvons faire le parallèle avec la tempête inflammatoire évoquée avec la Covid-19.
Une illustration concrète de ce phénomène est le développement du tissu lymphoïde péri-bronchique (hyperplasie du BALT). D’un côté, on peut le percevoir comme un élément positif car c’est la mise en œuvre des défenses immunitaires dans le tissu pulmonaire profond. Mais d’un autre côté, cette réponse du système immunitaire de l’animal a malheureusement pour effet de comprimer les bronchioles et de gêner la respiration (Figure 2).
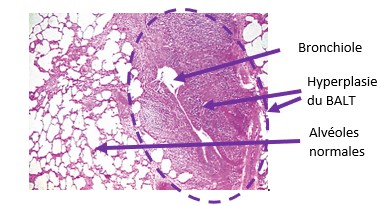 Figure 3 : photo d’histologie pulmonaire avec hyperplasie du tissu lymphoïde péri-bronchique (BALT) qui forme des nodules autour des bronchioles et les comprime (Vicca 2005)
Figure 3 : photo d’histologie pulmonaire avec hyperplasie du tissu lymphoïde péri-bronchique (BALT) qui forme des nodules autour des bronchioles et les comprime (Vicca 2005)
En conclusion, la destruction de l’escalator mucociliaire et les surinfections qui peuvent en découler, la toux, les difficultés respiratoires en lien avec la réponse immunitaire au sein du tissu bronchique expliquent comment Mhyo altère la santé et les performances des porcs.
Références bibliographiques
- Maes, Sibila et Pieters 2020. Mycoplasma in Swine. Acco Edition. Chapitre 3 : Mycoplasma hyopneumoniae pathogenicity : the known and the unknown. Pages 73-86
