Pendant longtemps, les infections à Mycoplasma hyopneumoniae (Mhyo) et la pneumonie enzootique ont été considérées comme une problématique concernant surtout les porcs charcutiers.
Il est en effet fréquent d’avoir une grande majorité de charcutiers positifs vis-à-vis de Mhyo. Et, quand la pathologie s’exprime en élevage, c’est le plus souvent en engraissement, au-delà de 60kg. De leur côté, les truies toussent peu et les rares fois où on inspecte leurs poumons à l’abattoir, peu de lésions sont visibles. Les infections à Mhyo ne concernent-elles que les porcs charcutiers ?
Aérotransmission avérée de Mhyo
C’est vraiment un élément qui ne fait aucun doute : des animaux contaminés excrètent Mhyo dans l’environnement, faisant de l’air un véhicule de transmission redoutable.
La démonstration de la transmission de Mhyo sur une longue distance a été faite aux Etats Unis, dans le Minnesota (Otake et al., 2010). La précision géographique a son importance car il faut imaginer un paysage de grandes plaines où rien n’arrête le vent. L’étude a consisté à réaliser des prélèvements d’air autour d’un bâtiment de 252 places très isolé hébergeant des porcs qui excrétaient Mhyo et du virus du SDRP. Contrairement à ce que l’on pensait jusqu’alors, Mhyo a diffusé loin puisqu’il a été retrouvé jusqu’à 9,2 kms de l’élevage ! Il s’agissait bien de pathogène infectieux car le Mhyo isolé a ensuite été inoculé à des porcs naïfs qui ont reproduit la maladie.


Photos : paysages du Minnesota
Notre environnement français ressemble assez peu à ces grandes plaines mais les situations hivernales durant lesquelles nous visualisons la condensation aux sorties d’air des élevages peut nous donner une idée des risques de transmission entre bâtiments d’élevage.
En ce qui concerne la transmission à l’intérieur des bâtiments proprement dit, l’ANSES a investigué et analysé l’air de six élevages atteints par le complexe respiratoire porcin et montré que Mhyo était le deuxième pathogène retrouvé le plus fréquemment dans l’air circulant après le virus influenza (Fablet et al., 2018).
- Les porcs contaminés sont donc une source de Mhyo dans les élevages. Même avec une conduite des salles en bande stricte, des charcutiers peuvent par transmission horizontale, par les flux d’air, contaminer des porcs plus jeunes, pas encore infectés.
- Le contrôle des circuits d’air en élevage est donc un enjeu pour contrôler Mhyo et les pathogènes respiratoires. Mais ce n’est pas la seule voie possible de contamination des porcelets.
Le rôle des reproducteurs dans la transmission de Mhyo
Sans doute du fait de sa capacité à produire des biofilms pour se « cacher » dedans et à déprimer localement les défenses immunitaires, Mhyo a un potentiel extraordinaire à persister à la surface de la trachée et des bronches des porcs atteints.
C’est ce qui a pu être mis en évidence avec le suivi dans le temps de cochettes de 15 semaines inoculées avec Mhyo et mises à plusieurs reprises en contact avec des cochettes naïves. Les cochettes inoculées ont commencé à tousser 2 semaines après inoculation mais ne présentaient plus de signes cliniques 10 semaines après. Néanmoins, 200 jours après inoculation, alors qu’elles ne présentaient plus aucun signe clinique, elles étaient toujours majoritairement positives et avaient donc transmis Mhyo aux cochettes naïves (Pieters et al., 2009). Le potentiel infectieux d’un porc contaminé par Mhyo va donc bien au-delà de la phase clinique et peut durer plus de six mois !
Aujourd'hui, beaucoup de cochettes d’élevages sont indemnes de Mhyo. C’est une bonne chose car elles ne vont pas apporter de nouvelle souche dans l’élevage d’accueil (plus il y a de souches dans un élevage, plus la pathologie est sévère ; Michiels et al., 2017). Mais quand ces cochettes se contaminent à l’entrée dans un élevage, cela veut dire qu’elles peuvent être excrétrices à leur mise-bas et contaminer leurs porcelets en maternité. C’est ce qui correspond à une dynamique d’infection précoce des porcelets par transmission verticale (truie-porcelet).
Deux études récentes ont montré qu’il n’était pas forcément rare d’avoir des cochettes porteuses de Mhyo.
- La première en Belgique a été réalisée dans dix élevages (Biebaut et al., 2022).
Les cochettes gestantes et en fin de première lactation se sont révélées plus fréquemment positives vis à vis de Mhyo que les truies multipares (Figure 1).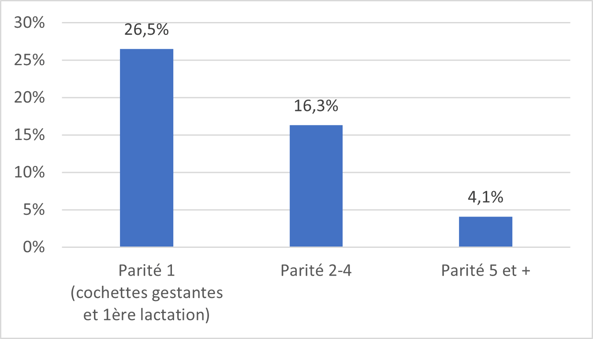
Figure 1 : Pourcentage de cochettes et truies positives vis-à-vis de Mhyo par sondage trachéobronchique (Biebaut et al., 2022). - La deuxième étude réalisée en France dans 20 élevages s’est focalisée sur des cochettes en fin de quarantaine et première moitié de gestation (Stynen et al., 2022). Il s’est avéré que 2/3 des élevages avaient des cochettes Mhyo positives sans que le statut « achat de cochettes » ou « auto-renouvellement » n’interfère. La question du portage de Mhyo par des reproducteurs ne se limite pas aux élevages achetant des cochettes négatives vis-à-vis de Mhyo.
En Conclusion
Le risque de transmission truies vers porcelets avant vaccination de ces derniers est donc une autre voie de contamination des porcelets à considérer. Il est important de ne pas négliger l'impact de cette transmission : en effet plusieurs études ont montré que la pathologie respiratoire est d’autant plus conséquente que le niveau de contamination des porcelets au sevrage est élevé (Fano et al., 2007 ; Fablet et al., 2013).
Références bibliographiques
- Biebaut et al., 2022. Influence of parity and reproductive stage on the prevalence of Mycoplasma hyopneumoniae in breeding animals in Belgian farrow‑to‑finish pig herds. Porcine Health Management, 8-26
- Fano et al., 2007. Effect of Mycoplasma hyopneumoniae colonization at weaning on disease severity in growing pigs. Canadian Journal of Veterinary Research. 71, 195-200
- Fablet et al., 2013. Relationships between cough, pneumonia-like gross lesions and Mycoplasma hyopneumoniae infection dynamics in 125 farrow-to-finish herds. Congrès ESPHM, Poster
- Fablet et al., 2018. Airborne detection of swine influenza A virus, PRRS virus and Mycoplasma hyopneumoniae in French swine herds. Congrès ESPHM, Poster HHM055
- Michiels et al., Impact of diversity of Mycoplasma hyopneumoniae strains on lung lesions in slaughter pigs. Michiels et al. Veterinary Research 48:2
- Otake et al., Long-distance airborne transport of infectious PRRSV and Mycoplasma hyopneumoniae from a swine population infected with multiple viral variants. Veterinary Microbiology 145, 198-208
- Pieters et al., 2009. An assessment of the duration of Mycoplasma hyopneumoniae infection in an experimentally infected population of pigs. Veterinary Microbiology 134, 261–266
- Stynen et al., Détection du Mycoplasma hyopneumoniae chez les cochettes de 20 élevages naisseurs engraisseurs. Congrès annuel AFMVP, 53-54
